La ferroportina
Una proteina, due diverse patologie: emocromatosi tipo 4 e deficit di ferroportina
La ferroportina 1 è una proteina che ha un ruolo fondamentale nel sistema di regolazione del metabolismo del ferro. È codificata dal gene SLC40A1 (Solute Carrier Family 40 Member 1), situato sul braccio lungo del cromosoma 2 (2q32.2) ed espresso in numerose linee cellulari.
La ferroportina è l'unica proteina, oggi nota, che regola l'uscita del ferro dalla cellula al sangue che, grazie all'azione della ceruloplasmina, si lega alla transferrina. Il suo ruolo è quindi determinante per mantenere adeguati livelli di ferro circolante nel sangue che, attraverso il legame con la transferrina, può così raggiungere i diversi siti di utilizzo e rilasciare in modo regolato il ferro alle cellule grazie al legame con lo specifico recettore 1 della transferrina (TFR1).
Anche se la ferroportina è espressa quasi ovunque, il ruolo fondamentale della proteina è quello svolto a livello delle cellule dell'epitelio intestinale, dove regola il rilascio del ferro dietetico dalla cellula duodenale al sangue, e a livello delle cellule macrofagiche della milza, dove regola il meccanismo di riciclo del ferro derivante dalla distruzione dei globuli rossi invecchiati.
Quest'ultima via è quella che ricicla la quasi totalità del ferro che viene mobilizzato giornalmente (circa 20-25 mg, rispetto agli 1-2 mg assorbiti a livello intestinale) e che permette di soddisfare le esigenze dei diversi tessuti e in particolare del midollo eritroide (quello che produce i globuli rossi), principale utilizzatore del ferro dal punto di vista quantitativo.
La ferroportina è a sua volta regolata per garantire questo adeguato flusso di ferro evitando nello stesso tempo che possa accumularsi in quantità eccessive rispetto alle necessità. La proteina che regola l'azione della ferroportina è l'epcidina, un piccolo peptide sintetizzato dal fegato in funzione del fabbisogno di ferro: in caso di maggior fabbisogno la sintesi di epcidina viene ridotta e vicerversa, poiché l'epcidina esercita un'azione inibitoria sulla funzione della ferroportina.
In pratica, l'epcidina si lega alla ferroportina presente sulla membrana cellulare e ne blocca la funzione oppure la internalizza e ne favorisce la degradazione. Questa azione fa sì che il numero di molecole di ferroportina funzionanti presenti sulla membrana delle cellule (dei macrofagi e dell'epitelio intestinale) si riduca e, conseguentemente, diminuisca anche la capacità di esportare ferro nel sangue. L'opposto accade se la quantità di epcidina circolante si riduce, poiché in questo caso un numero maggiore di molecole di ferroportina sarà presente sulla membrana cellulare pronta a rilasciare ferro nel sangue (per ulteriori dettagli vedere Il metabolismo del ferro).
Come già descritto nell'articolo L'emocromatosi, mutazioni a carico del gene SLC40A1 possono dare origine a due forme diverse di patologia da sovraccarico di ferro: l'emocromatosi tipo 4 (SLC40A1-HC), dovuta a mutazioni cosiddette gain-of-function, e il deficit di ferroportina, dovuto a mutazioni loss-of-function. Entrambe hanno una trasmissione di tipo dominante, cioè basta un singolo difetto genetico (e quindi un solo genitore affetto) per trasferire la malattia ai figli con una probabilità del 50%. Tuttavia, le due patologie sono molto diverse tra loro e oggi il deficit di ferroportina non è più annoverato tra le forme di emocromatosi, ma costituisce un'entità distinta tra le patologie da sovraccarico di ferro.
Emocromatosi tipo 4
Dell'emocromatosi tipo 4 si è già parlato nell'articolo L'emocromatosi. In breve, le mutazioni responsabili determinano una resistenza all'azione dell'epcidina, che non è più in grado di esercitare il proprio effetto inibitorio tramite il blocco e la degradazione della ferroportina. Il risultato è un'aumentata presenza di molecole di ferroportina sulla membrana (cellulare) e quindi un aumentato rilascio di ferro nel sangue da parte delle cellule duodenali e dei macrofagi, con aumento della saturazione della transferrina e progressivo accumulo di ferro nel fegato e nei diversi tessuti.
Si realizza quindi un quadro clinico simile alle altre forme di emocromatosi, che si manifesta in età adulta con caratteristiche paragonabili alla forma più comune (emocromatosi tipo 1 o HFE-HC). Nella figura 1 è schematizzato il meccanismo che caratterizza questa forma di emocromatosi.
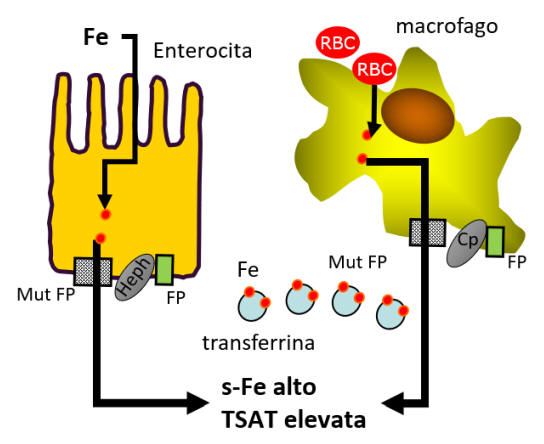
Figura 1. Le mutazioni “gain-of-function” della ferroportina inducono un aumento
della funzione della proteina e un aumentato rilascio di ferro nel sangue.
FP: ferroportina – Heph: efestina – Cp: ceruloplasmina – s-Fe:
ferro plasmatico – TSAT: saturazione della transferrina.
Deficit di ferroportina
Più frequentemente, le mutazioni del gene SLC40A1 causano una perdita di funzione (loss-of-function) della ferroportina. In questo caso la proteina mutata non raggiunge la membrana cellulare e il risultato è una ridotta capacità di esportare ferro, che rimane quindi in parte intrappolato nelle cellule. Questo determina lo sviluppo di un accumulo di ferro prevalentemente a carico delle cellule macrofagiche, ma non sufficiente a determinare una carenza di ferro circolante in condizioni standard.
Nella figura 2 è schematizzato il meccanismo che caratterizza questa patologia.
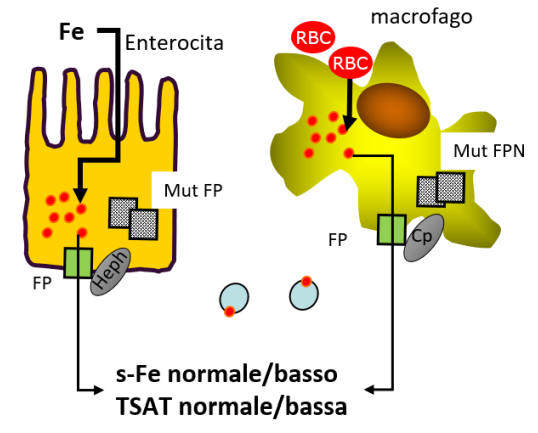
Figura 2. Le mutazioni “loss-of-function” della ferroportina inducono
una ridotta funzione della proteina e un ridotto rilascio di ferro nel
sangue.
Dal punto di vista clinico, le principali differenze tra deficit di ferroportina ed emocromatosi sono:
- la concentrazione del ferro circolante è normale;
- la saturazione della transferrina è normale e non aumentata come nell'emocromatosi;
- il sovraccarico di ferro coinvolge prevalentemente le cellule del sistema reticolo-endoteliale (macrofagi) ed eventualmente solo tardivamente gli epatociti.
A causa dell'accumulo prevalente nei macrofagi, le concentrazioni di ferritina sono spesso elevate o molto elevate in misura sproporzionata rispetto alla reale concentrazione di ferro epatico. Dal punto di vista clinico, anche se la malattia presenta una discreta variabilità individuale, le manifestazioni sono generalmente modeste e le complicanze d'organo risultano poco frequenti.
Per orientarsi meglio rispetto al solo dosaggio della ferritina può essere utile eseguire una risonanza magnetica dedicata per quantificare il ferro nel fegato e nella milza (vedere articolo Biopsie magnetiche).
Anche la terapia, basata sulla salassoterapia, deve essere gestita in modo differente rispetto all'emocromatosi classica. I salassi devono essere eseguiti con una frequenza adeguata alla ridotta capacità dei macrofagi di rilasciare ferro, lasciando il tempo necessario alla ricostituzione dei globuli rossi rimossi.
Un approccio troppo intensivo può infatti determinare un deficit di ferro funzionale (bassi livelli di ferro e saturazione della transferrina nonostante ferritina ancora elevata) e anemia. Per questo, generalmente, si imposta un regime più blando, con un salasso mensile, valutando progressivamente la risposta clinica e laboratoristica.
Poiché nel deficit di ferroportina l'accumulo interessa soprattutto i macrofagi e solo modestamente i parenchimi, questo approccio più conservativo non rappresenta un rischio per il paziente. Tuttavia, se la risonanza magnetica evidenzia un accumulo epatico significativo, la salassoterapia può essere modulata caso per caso, sempre sulla base della risposta clinica e degli esami di laboratorio.
prof. Alberto Piperno
[Articolo pubblicato il 14-09-2003 e aggiornato il 05-11-2023]