Una patologia con accumulo di ferro cerebrale: l'aceruloplasminemia
Il ferro è un metallo bioattivo essenziale; partecipa a moltissime funzioni
in tutto l'organismo. A livello cerebrale, il ferro svolge funzioni essenziali
nei processi di:
- biosintesi di neurotrasmettitori (sostanze che veicolano le informazioni fra le cellule componenti il sistema
nervoso);
- formazione della mielina (la sostanza che riveste, isola e protegge le fibre nervose);
- metabolismo energetico.
Tuttavia, l'eccesso di ferro nel cervello può causare danni neuronali e morte cellulare, perché il ferro (Fe2+) aumenta lo stress ossidativo mediante la generazione di radicali liberi altamente citotossici.
Esiste un gruppo di patologie neurodegenerative (sindromi NBIA, acronimo di Neurodegeneration of the Brain with Iron Accumulation: neurodegenerazione cerebrale con accumulo di ferro) caratterizzate da un accumulo di ferro prevalente in alcune sedi particolari del cervello: i nuclei o gangli della base localizzati alla base di entrambi gli emisferi cerebrali e densamente interconnessi con la corteccia cerebrale e altre strutture come il talamo e il tronco dell'encefalo (Figura 1).
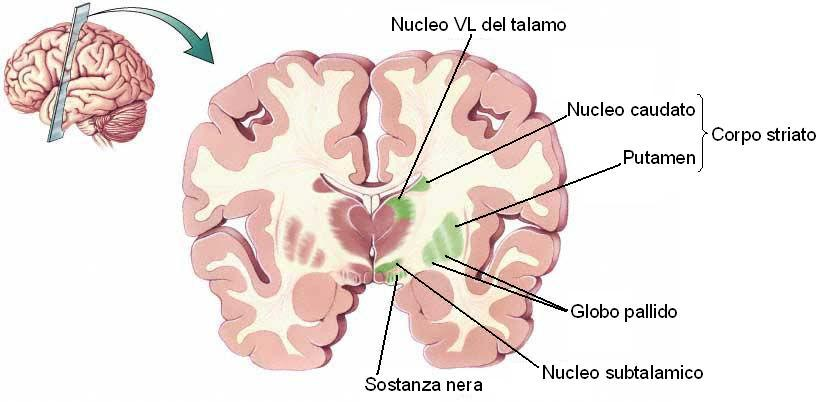
Figura 1: Sezione e anatomia del cervello.
Essi sono coinvolti principalmente nel controllo del movimento, ma anche negli aspetti motivazionali, emozionali e di attenzione che guidano i movimenti finalizzati. A supporto di questo ruolo, studi autoptici (post mortem) nell'uomo hanno riscontrato alterazioni patologiche nei nuclei della base in diverse malattie neurologiche degenerative tra cui il morbo di Parkinson e la corea di Huntington.
Le sindromi NBIA si manifestano clinicamente con un progressivo disturbo del movimento con comparsa di movimenti involontari (corea) e progressiva incapacità di mantenere il coordinamento motorio e una corretta deambulazione come sintomi principali. A livello tissutale si osserva una progressiva degenerazione sia dei neuroni (le cellule cerebrali per eccellenza) che degli astrociti (le cellule nervose che servono da impalcatura e da supporto alle funzioni dei neuroni).
Tra le sindromi NBIA, quelle direttamente imputate a difetti nei geni ferro-correlati ci sono la neuroferritinopatia e l'aceruloplasminemia (ACP) causate da mutazioni a carico del gene della ferritina L (FTL) e della ceruloplasmina (CP), rispettivamente.
Il primo caso di ACP (OMIM, #604290) è stato documentato in Giappone nel 1987 da Miyajima H, che ha descritto una donna di 52 anni affetta da disturbi dell'attività muscolare palpebrale (blefarospasmo), degenerazione retinica, diabete mellito, anemia microcitica (globuli rossi piccoli) con bassi livelli di ferro nel sangue ma elevati livelli di ferritina. La paziente presentava un accumulo di ferro nel cervello (valutato mediante risonanza magnetica), nel fegato e nel pancreas e l'assenza della ceruloplasmina plasmatica (Cp). Successive analisi hanno rivelato la presenza di una mutazione in omozigosi nel gene CP, localizzato sul cromosoma 3q23.
La ceruloplasmina è una rame-ossidasi e contiene il 95% del rame presente nel siero umano. Viene inizialmente sintetizzata come apo-proteina (priva di rame) che, quando lega sei atomi di rame, si modifica nella forma olo (chiamata ceruloplasmina) (Figura 2).
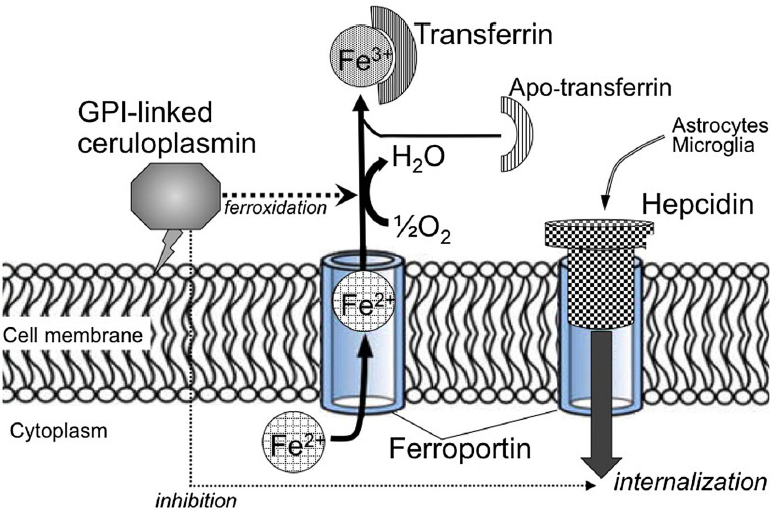
Figura 2: Biosintesi della ceruloplasmina (tratto da Kono S, 2013).
Esistono due forme distinte di Cp (isoforme) generate dal medesimo gene: una forma secreta nel sangue (ceruloplasmina sierica) lunga 1040 aminoacidi e una forma di membrana (GPI-linked) contenente 25 aminoacidi in più. L'isoforma secreta è espressa solo negli epatociti, mentre la forma GPI è espressa nel cervello, fegato, polmoni, reni e molti altri organi.
La malattia ACP rivela il ruolo della Cp nell'omeostasi del ferro. Essa svolge un'importante funzione nel processo che regola l'efflusso del ferro dalle cellule attraverso la ferroportina (la proteina che svolge il ruolo di esportatore del ferro). Infatti la Cp, ossidando il ferro ferroso Fe2+ a ferro ferrico Fe3+, favorisce il legame del ferro alla transferrina extracellulare (Figura 3).
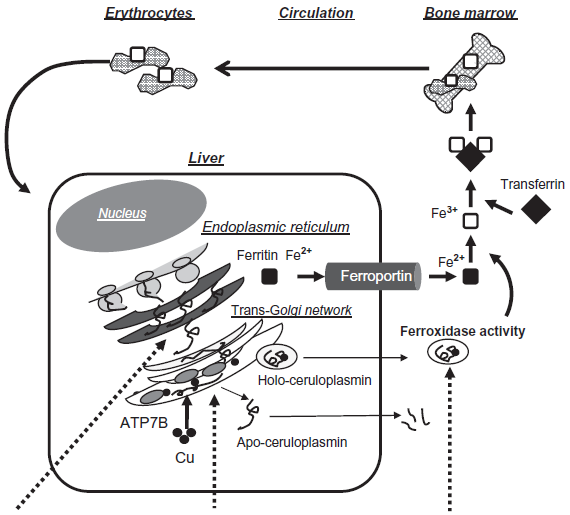
Figura 3: Trasporto del ferro a livello della membrana degli astrociti (tratto da Miyajima H, 2015).
La ferroportina è regolata a livello post-traduzionale attraverso la sua internalizzazione e successiva degradazione ad opera dell'epcidina. Studi di De Domenico et al. nel 2007 hanno dimostrato che l'attività ferrossidasica della GPI-CP è essenziale per la stabilità in membrana della ferroportina nelle linee murine di glioma. Il ridotto rilascio di ferro alla transferrina, conseguenza della disfunzione della ceruloplasmina, determina le manifestazioni classiche della patologia:
1. anemia microcitica ferro-carenziale;
2. accumulo di ferro tissutale sia a livello sistemico che cerebrale.
A sua volta l'anemia ferro-carenziale determina modificazioni nella sintesi di epcidina (l'ormone regolatore del metabolismo del ferro), aumentando l'assorbimento del ferro a livello intestinale. Ciò contribuisce ad aumentare l'accumulo di ferro cellulare, esacerbando la patologia.
Lo stesso meccanismo avviene a livello cerebrale, dove la GPI-CP legata alla membrana degli astrociti trasforma il Fe2+ in Fe3+, permettendone il trasporto ai neuroni tramite transferrina. Nel cervello inoltre la ceruloplasmina svolge un importante ruolo antiossidante, preservando il sistema nervoso centrale dai danni mediati dai radicali liberi (•OH) formatisi in seguito alla Reazione di Fenton tra lo ione Fe2+ e H2O2.
Da un punto di vista clinico, l'ACP è l'unica tra le sindromi da sovraccarico di ferro che coinvolge sia il ferro sistemico sia il metabolismo cerebrale. Le manifestazioni cliniche sono caratterizzate dalla cosiddetta triade: degenerazione retinica, diabete mellito e segni neurologici.
Dr.ssa Sara Pelucchi
[Articolo pubblicato il 05-05-2018]